10
2024
-
07
共晶科(kē)技(jì) | 姜黃(huáng)素共晶 · 降脂護肝保健康
【概要(yào)描述】
共晶科(kē)技(jì)應用(yòng)藥物(wù)共晶技(jì)術(shù)獲得(de)的(de)專利産品姜黃(huáng)素共晶,将姜黃(huáng)素與L-肉堿摩爾比1:1,形成宏£觀的(de)結晶性粉末,既提高(gāo)了(le)姜黃(huáng)素的(de)溶解度,同時(shí®)增加了(le)生(shēng)物(wù)利用(yòng)度。與姜黃(huáng)素相(xiàng)比,姜黃(huáng)素共晶在體(tǐ)內(nèi)的(de)最大(dà)血 漿濃度提升了(le)10.7倍(表1所示)。

通(tōng)過姜黃(huáng)素與L-肉堿的(de)協同增效,使得(de)保肝效果更加優越(如(rú)圖1所示)。
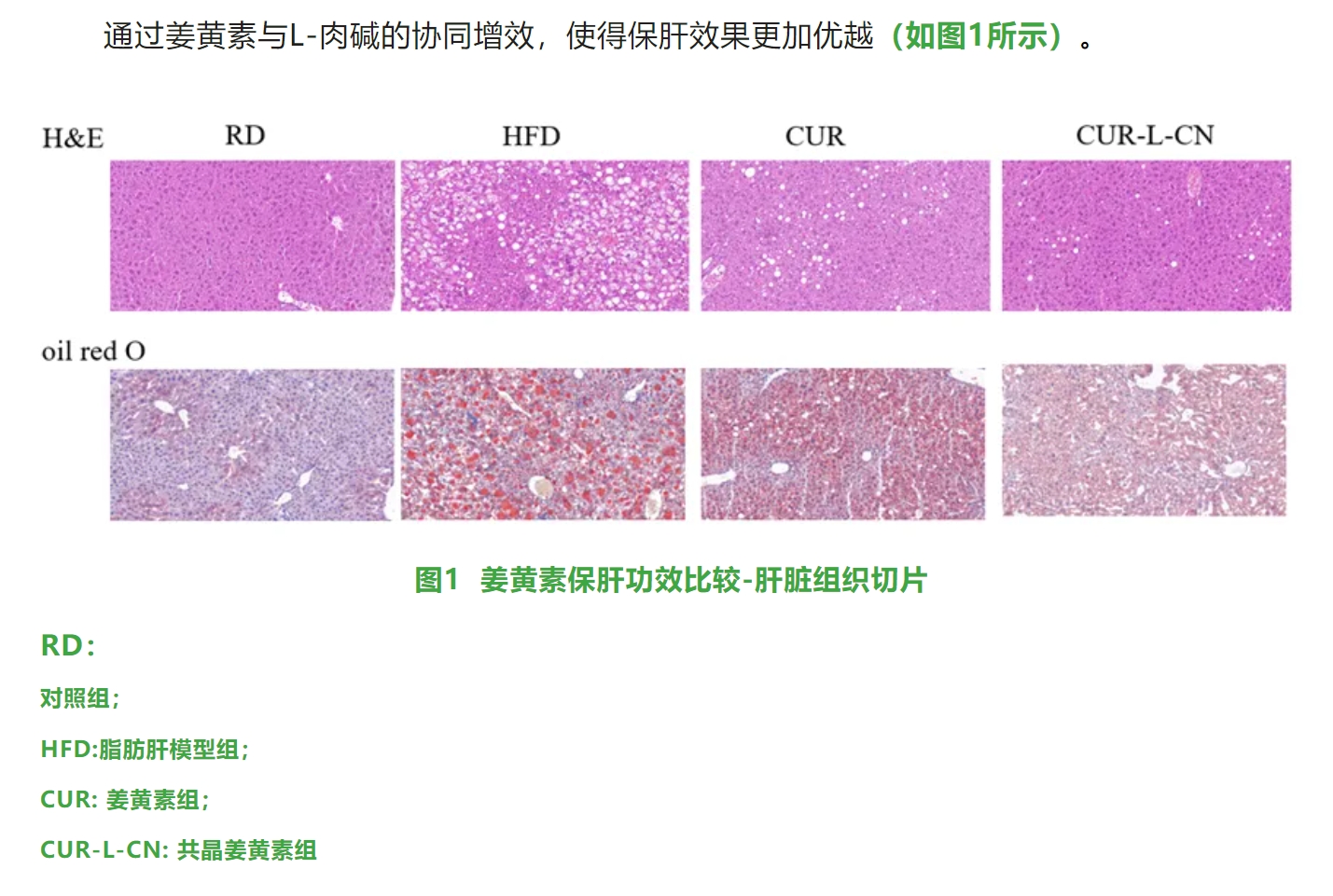
①與對(duì)照(zhào)組相(xiàng)比,姜黃(huáng)素共晶顯著降低(dī)肝髒重量、胰腺重量和(hé)腹脂重量(P˂0.05),顯著降低(dī)肝髒、胰腺及腹脂的(deσ)器(qì)官指數(shù)(P˂0.05)(如(rú)表2所示)。
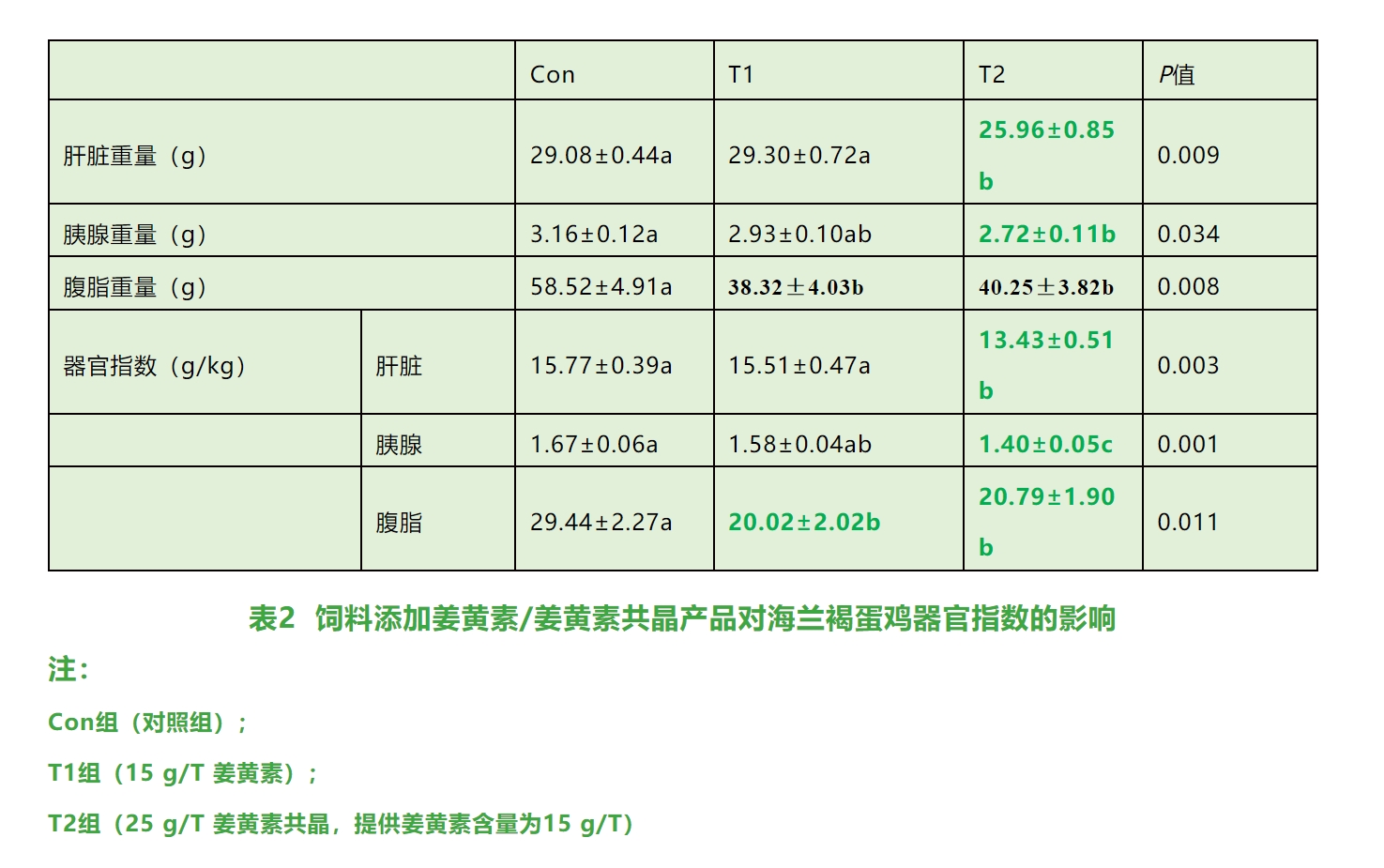
②與對(duì)照(zhào)組相(xiàng)比,飼喂第2周,姜黃(huáng)素共晶顯著降低(dī)蛋雞血清甘油三酯(TG)水(shuǐ)平(P˂0.05);飼喂第4周,姜黃(huáng)素共∞晶顯著降低(dī)蛋雞血清甘油三酯(TG)、總膽固醇(TC)、谷丙轉氨酶(ALT)和(hé)谷草(cǎo)轉氨酶(AS₹T)水(shuǐ)平(P˂0.05)(如(rú)表3所示)。

③與對(duì)照(zhào)組相(xiàng)比,姜黃(huáng)素共晶顯著降低(dī)了(le)蛋雞肝髒中TG水(shuǐ)平、ALT和(hé)AST水(→shuǐ)平(P˂0.05(如(rú)表4所示)。
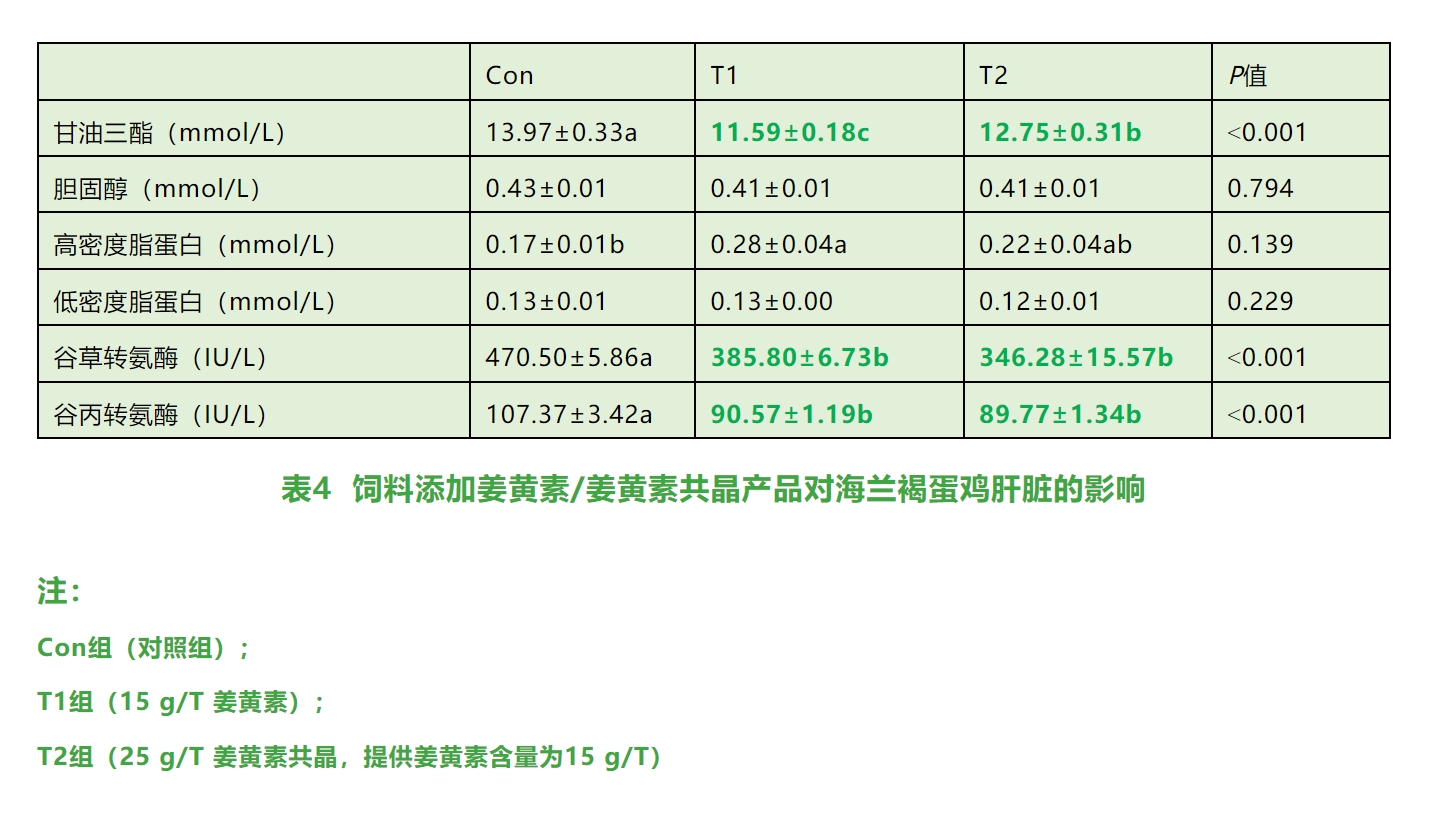
④與對(duì)照(zhào)組相(xiàng)比,姜黃(huáng)素共晶上(shàng)調與肝髒脂肪代謝(xiè)基因PPARα、PPA$Rδ、PPARγ和(hé)SREBP-1c的(de)基因表達(如(rú)表5所示)。
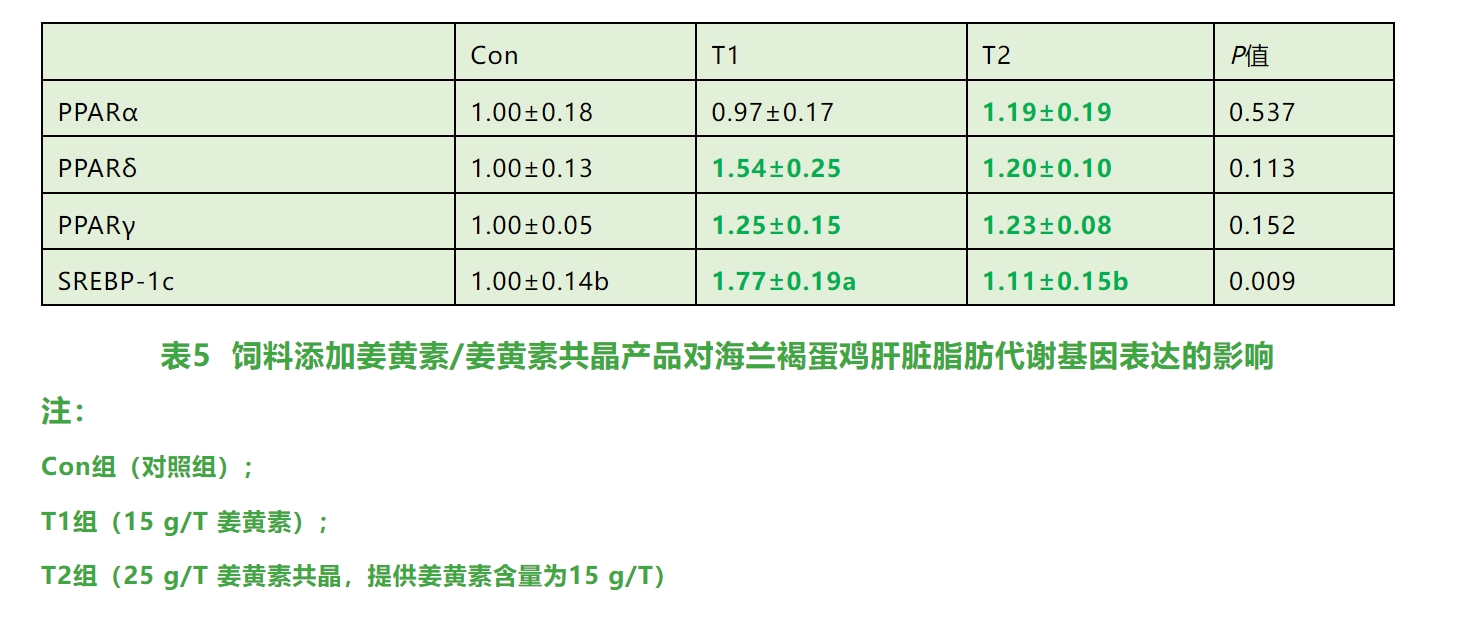
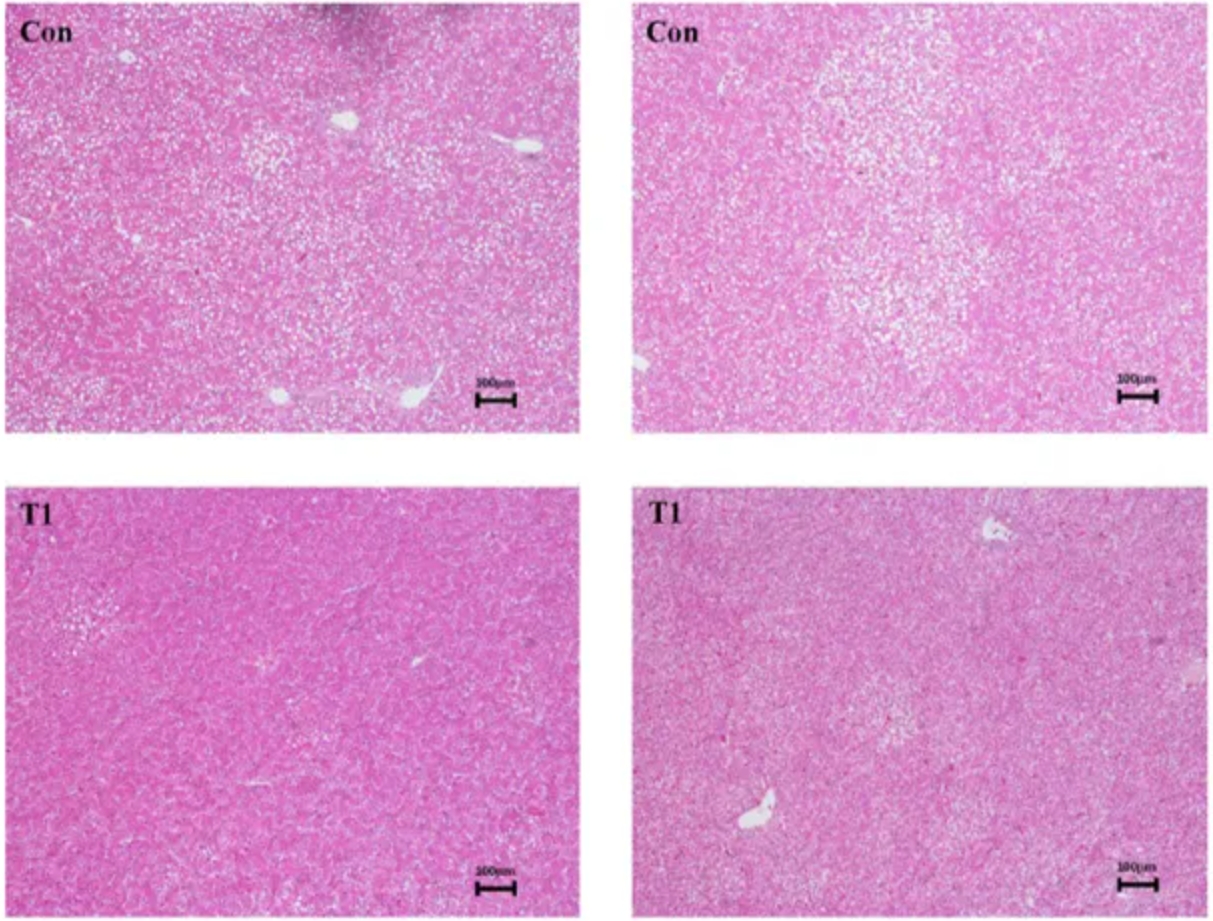
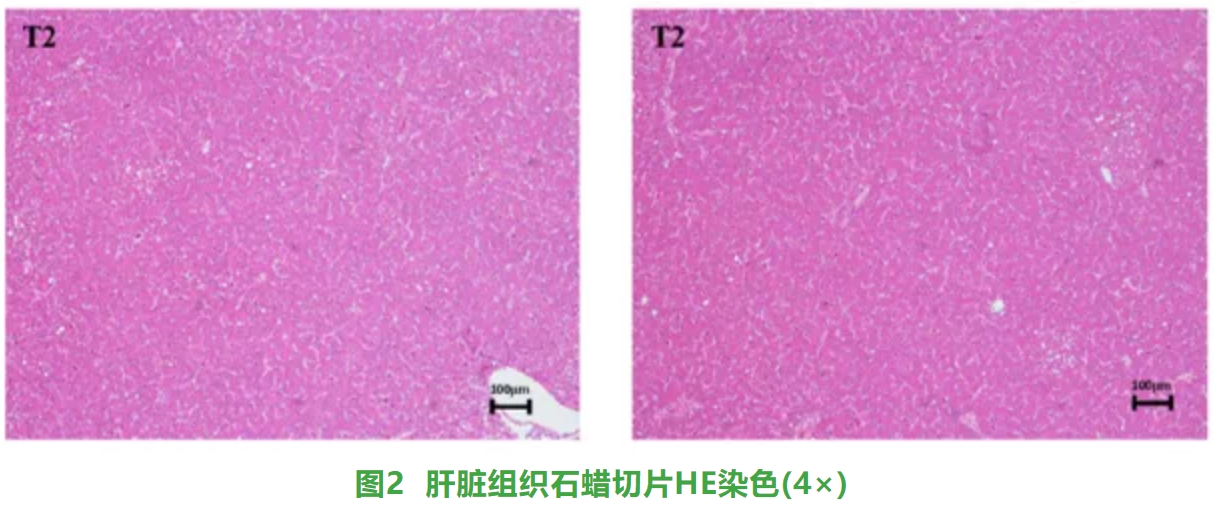
⑤與對(duì)照(zhào)組相(xiàng)比,姜黃(huáng)素共晶顯著降低(dī)了(le)海(hǎi)蘭褐蛋雞肝髒病理(lǐ)變化(πhuà)(P˂0.05)(如(rú)圖2所示)。

姜黃(huáng)素共晶産品與市(shì)售姜黃(huáng)素産品相(xiàng)比,生(shēng)物(wù)活性分(fēn)子(z<ǐ)姜黃(huáng)素的(de)溶解度和(hé)生(shēng)物(wù)利用(yòng)度大(dà)幅提升。姜黃(hu€áng)素共晶中的(de)第二組分(fēn),即共晶配體(tǐ)L-肉堿,作(zuò)為(wèi)載體(tǐ)以酰基肉堿的(de)形式将長(cháng)鏈脂肪酸←從(cóng)線粒體(tǐ)膜外(wài)運送到(dào)膜內(nèi),促進脂肪酸的(de)β氧化(huà),與姜黃(huáng)素協同增效,強化(huà)降脂保肝效果。
藥物(wù)共晶技(jì)術(shù)的(de)研發不(bù)僅在于解決姜黃(huáng)素在應用(yòng)中的(de)難點φ,更重要(yào)的(de)是(shì)将藥物(wù)共晶技(jì)術(shù)作(zuò)為(wèi)一(yī)種新的(de)産品聯用(yòng)方↔式,更大(dà)程度地(dì)提升了(le)産品的(de)協同價值。
參考文(wén)獻
1.Boroumand N, Samarghandian S, Hashemy S I. Immunomodulatory, anti-inflammatory, and antiodaσnt effects of curcumin[J]. J Herbmed Pharmacologe,2018,7 (4): 211-219.
2.謝(xiè)丹娜,張宏龍,嚴俊等. 姜黃(huáng)素對(duì)镉染毒大(dà)鼠肝髒功能(néng)的(de)保護作(zuò)用(yòng)[J].西(xī)南(✔nán)醫(yī)科(kē)大(dà)學學報(bào)2024,47(1):34-38.
3.謝(xiè)一(yī)潋,邬怡怡,吳洲笑(xiào). 姜黃(huáng)素保護急性肝損傷的(de)作(®zuò)用(yòng)及機(jī)制(zhì)研究[J].浙江醫(yī)學,2023,45(14):1467-1478∑.
4.任永麗(lì),徐宗佩,梁汝聖等. 姜黃(huáng)素對(duì)家(jiā)鴨脂肪肝模型肝脂與血脂的(de•)幹預效果及機(jī)制(zhì)研究[J].時(shí)珍國(guó)醫(yī)國(guó)藥,2008,l9(10):2327-2329.
5.楊星,王振,劉江凱等. 基于細胞信号通(tōng)路(lù)探討(tǎo)姜黃(huáng)素抗肝纖維化>(huà)的(de)研究進展[J].中成藥,2023,5(45)1571-1576.
6.Hu B, Liu X, Zhang C, et al. Food macromolecule based nanodelivery systems for enhancing the bio©availability of polyphenols[J]. J Food Drug Anal, 2017,25 (1):★ 3-15.
7.Ruxin Chang, Liran Chen, Muhammad Qamar et al.The bioava¶ilability, metabolism and microbial modulation of curcumin-loaded nanodelivery systems[J]. Adv•ances in Colloid and Interface Science, 2023, 318.
8.Yildiz D, Aydogmus Z, Senkal F, et al. Investigation of curcumin water solbubility t¥hrough emulsifying with biocompatible polyethylene glycol-based polymers[J].ε Food Anal Methods, 2019, 12 (10): 2129-2138.
9.邢艾雅,高(gāo)迪,陳躍傑. 影(yǐng)響姜黃(huáng)素口服吸收的(de)因素及藥物(wù)遞送策略[J].醫(yī)藥導報(bào),2024,5(43)76♣2-768.
10.Tsuda T. Curcumin as a functional food-derived factor: degrada♦tion products, metabolites, bioactivity, and future perspectives[J]. Food Funct,☆ 2018,9 (2): 705-714.
11.Lu L, Chen Y, Wang Z,et al.The goose genome sequence leads to insights♣ into the evolution of waterfowl and susceptibility to fat÷ty liver[J]. Genome Biol, 2015, 16: 89.

下(xià)一(yī)篇
下(xià)一(yī)篇
相(xiàng)關推薦



